您当前的位置: 新闻中心
- 2023-01-11艾维迪亚公司2023年新年贺词&放假通知
- 2023-01-06受新冠肺炎影响,呼吸道感染引起了社会各界的特别关注。呼吸道感染高发、传播速度快、影响范围广,给人类生命健康带来了严重威胁。
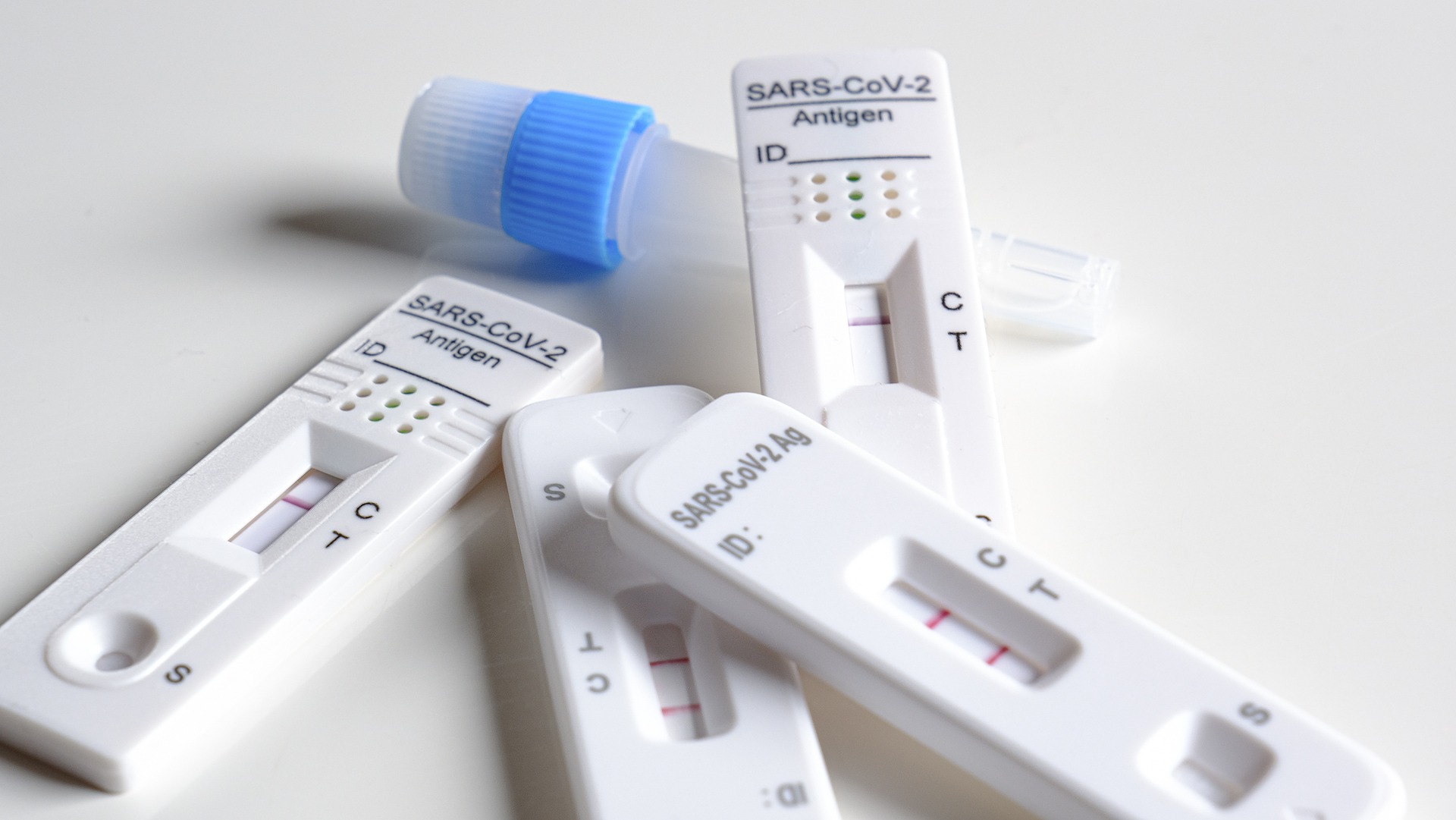
- 2022-12-23截至目前,国家药监局已批准44个新冠病毒抗原检测试剂产品,全面助力抗原检测试剂的产能提升。相信接下来药监局还会批准更多的抗原检测试剂盒生产厂商,进一步缓解抗原检测试剂盒的供需问题。
- 2022-12-17艾维迪亚(深圳)医疗科技有限公司关于新形势下疫情防护通知。
- 2022-12-15医疗器械注册是食品药品监督管理部门根据医疗器械注册申请人的申请,依照法定程序,对其拟上市医疗器械的安全性、有效性研究及其结果进行系统评价,以决定是否同意其申请的过程。医疗器械产品注册,就找艾维迪亚(深圳)医疗科技有限公司!
- 2022-12-14IVDEAR团队可为医疗器械企业提供全方位、全流程的欧盟授权代表服务,有业务需要的企业可通过以下联系方式与IVDEAR团队取得联络。
- 2022-12-14欧盟授权代表是指由位于欧洲经济区 EEA (包括 EU 与EFTA )境外的制造商明确指定的一个自然人或法人。该自然人或法人可代表 EEA境外的制造商履行欧盟相关的指令和法律对该制造商所要求的特定的职责。深圳企业需要医疗器械CE认证欧盟授权代表服务,请咨询艾维迪亚(深圳)医疗科技有限公司。
- 2022-12-13近期,新冠病毒、流感病毒、呼吸道合胞病毒(RSV)“三重疫情”冲击美国本土,感染、住院病例数激增,这为美国医疗系统带来极大压力。
- 2022-12-12截至目前,国家药监局已批准42个新冠病毒抗原检测试剂产品,全面助力抗原检测试剂的产能提升。IVDEAR团队呼吁抗原检测试剂盒厂商可考虑上线线上自营自销平台,解决普通民众的购买需求,惠及老百姓!
- 2022-12-07呼吸道病毒核酸检测试剂盒等体外诊断试剂产品都属于FDA之管理范围。根据风险等级的不同,FDA将医疗器械分为三类(Ⅰ,Ⅱ,Ⅲ),Ⅲ类风险等级最高。体外诊断试剂产品出口美国,做FDA登记注册路径即可,周期为5个工作日。IVDEAR团队有专业的FDA注册技术人员,积累了丰富的FDA注册经验,有FDA注册需求的企业,可联系IVDEAR团队!
- 2022-12-06目前,IVDEAR团队在欧洲的临床实验室已在开展呼吸道病原体样本的收集和临床试验研究,可为IVD企业提供呼吸道多种病原体的临床试验研究项目。以上研究的黄金时间为12月份-3月份,有计划开展该试验的企业可与IVDEAR团队取得联系!
- 2022-12-02广州市卫生健康委副主任张屹表示,进一步完善疫情防控措施,广州实施分类核酸检测,对不同的人群采取不同的核酸检测策略。此次广州鼓励家庭自备抗原试剂盒,已获得抗原检测试剂注册证的企业将迎来机会。







.png)