近日,圣湘生物自主研发的猴痘病毒核酸检测试剂盒(PCR-荧光探针法)通过英国MHRA认证,该产品获得英国MHRA注册后,可在英国和认可英国MHRA注册的国家或地区销售,这是继欧盟CE之后斩获的又一权威认证。

截至2022年8月18日,WHO统计全球94个国家和地区已报告近4万例猴痘病例,早先总干事谭德塞宣布猴痘疫情为"国际关注的突发公共卫生事件"。
猴痘病毒潜伏期较短,传播速度快,传播方式复杂,美国,西班牙,巴西,德国,英国等欧美国家猴痘疫情相对严重,我们的邻近国家泰国、越南等出现病例,我国台湾地区也发现猴痘病例,需要警惕猴痘病毒在我国的传播风险。
为什么现在就要办英国MHRA注册?
目前英国UKCA认证仍处于过渡期, 在2023年7月1日前,中国厂家可以通过原有的CE证书,联系IVDEAR快速完成英国注册。2023年7月1日后,英国将全面启动UKCA认证,原有的CE证书将得不到英国认可,必须通过英国的UKCA公告机构来完成英国认证。
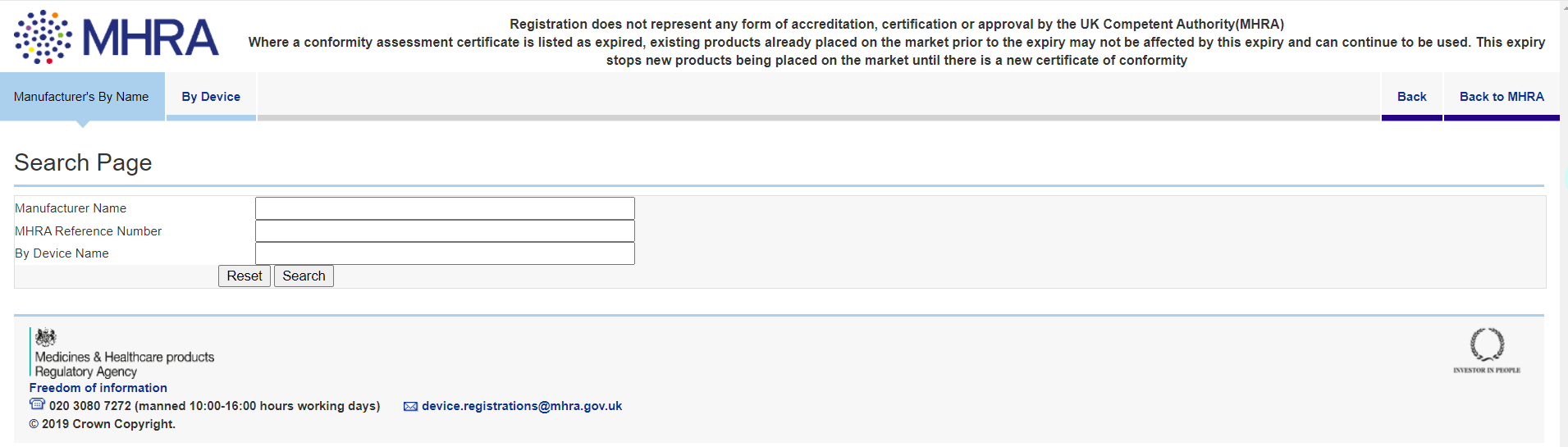
MHRA公众数据库查询界面
完成UKCA注册后约1周时间,厂家信息将公布到MHRA公众数据库,供英国的经销商和进口商查询,帮助经销商和进口商快速和英国客户建立联系。
查询链接:https://aic.mhra.gov.uk/era/pdr.nsf/Search?openform
同时,其注册的产品,也将在1~2个月后公布到这个网站。
IVDEAR · 专业注册咨询机构
IVDEAR(艾维迪亚)是国瑞中安集团旗下重点培育品牌-位于深圳光明新区分支机构。依托国瑞中安集团强有力的资源、渠道和专业背景,IVDEAR专注于为国内外各大企业提供全球各国医疗器械合规化咨询全过程、全方位服务,致力于协助和支持中国本土企业迈向全球化、合规化。
IVDEAR团队在注册认证行业从业多年,积累了大量的行业经验和资源,以注册认证市场为导向,为客户提供高效、实用、高价值且符合各项目需求的解决方案。
有需进一步了解英国MHRA认证的企业可与IVDEAR团队取得联络。


